张通社 zhangtongshe.com
|立足张江,面向上海,服务科创|
1月28日,成都康华生物(维权)制品股份有限公司(300841.SZ,以下简称“康华生物”)召开董事会,宣布与纳美信(上海)生物科技有限公司(以下简称“纳美信”)创始团队及现有股东签署框架文件,约定通过分期认购新增注册资本及受让股权的方式,最终实现对纳美信生物100%控股。
本次整合并非传统意义上的“退出”路径,而是一家拥有深厚技术积淀的创新型biotech,在其发展的关键节点,选择与成熟产业平台深度融合的战略决策。
这不仅仅是一次资产的并购重组,更体现了研发能力与产业能力的结构性互补——纳美信生物以其在mRNA冻干工艺与AI驱动抗原设计上的突破,补强了康华生物下一代疫苗技术平台;而康华生物则以其产业化、质量控制和商业化网络优势,为前沿技术提供了通往患者的价值通路。
ZHANG TONG SHE
PART.01
纳美信生物:
在mRNA赛道上坚持差异化研发定力
纳美信成立于2021年,是一家专注于mRNA领域新型疫苗与药物研发的创新生物技术企业。一直以来,公司秉承“AI驱动、源头创新”的研发理念,聚焦具有明确临床未满足需求的疾病领域,致力于打造一个具备持续创新能力的mRNA技术平台。
公司创始团队拥有20多年病毒学、免疫学和疫苗领域的积累,核心团队曾在海内外顶尖研究机构、MNC担任要职,具备完整mRNA领域的研发及产业化经验:
公司联合创始人、CSO钱志康博士深耕疱疹病毒分子机制研究逾二十年,是国内最早探索mRNA疫苗应用的科学家之一;CMC负责人刘军博士曾在赛诺菲、优时比等企业领导生物药工艺开发、分析方法验证与注册申报工作;研发副总裁马光刚博士曾任职于勃林格殷格翰、先声祥瑞,领导过多条mRNA项目管线的临床前研发工作。
在短短几年时间内,纳美信快速搭建起覆盖靶点筛选、抗原设计、mRNA序列优化、LNP递送系统开发、冻干制剂工艺及药理药效评价的全链条技术平台。其核心技术平台包括:
基于AI的抗原与密码子优化工具(包括自主知识产权的CodonBox、AntigenBoost),提升mRNA翻译效率与蛋白表达稳定性;
突破性的mRNA-LNP冻干工艺,实现产品在2–8℃条件下的长期稳定储存;
结合新型可电离脂质的LNP递送体系,更好适配纳美信自主开发的冻干工艺,全面提升产品的安全性和免疫原性。
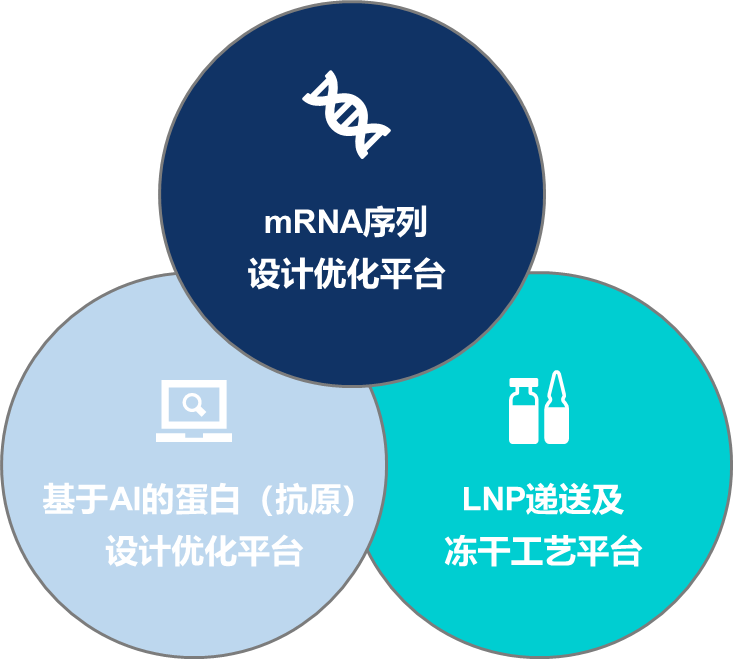 图1:纳美信mRNA核心技术平台
图1:纳美信mRNA核心技术平台围绕上述技术平台,纳美信构建了完善的知识产权体系,全面覆盖序列设计、递送系统及产业化工艺。截至目前,纳美信已申请14项发明专利(含1项PCT国际专利,10项已公开),并取得6项软件著作权登记证书。
在序列设计方面,公司针对mRNA关键调控元件(3‘UTR、5’UTR、poly(A)尾)及密码子优化算法进行了系统性专利布局,实现更高效、稳定的蛋白表达;另一方面,针对海外核酸药物龙头企业的专利封锁,公司构建了全新可电离阳离子脂质分子库,并筛选出结构新颖、高效低毒的可电离阳离子脂质分子,相关专利已公开。此外,公司在靶向递送方向上也积累了比较好的技术储备。
mRNA药物产业化面临的核心挑战之一在于其稳定性。单链RNA分子的2'-OH亲核基团使其在水相中易水解,因此mRNA新冠疫苗需采用超低温冷链运输以维持稳定。但国内和大部分发展中国家,并不具备完善的疫苗低温/超低温供应链条件,若想将mRNA平台拓展至流感、RSV等常规品种并下沉至发展中国家,就应该设法将产品储运条件提高至2–8℃,并达到2年以上长期稳定,这是mRNA疫苗工艺难点,即纳美信自设立初期投入冻干平台技术开发的原因。
在这一行业背景下,公司自主开发了国内领先的冻干工艺,实现了包埋、超滤浓缩、冻干保护剂及工艺参数等多环节突破,解决了现有疫苗产品需超低温储运的痛点,也为产品管线开发与迭代提供了坚实、自主的基础。
公司核心在研品种呼吸道合胞病毒(RSV)mRNA疫苗NR222,2024年12月获得国家药监局药品审评中心(CDE)临床试验默示许可(受理号:CXSL2400681),成为国内首个申报临床的冻干剂型mRNA疫苗品种,标志着公司在mRNA技术创新与产业化路径上迈出关键一步。
纳美信开发的呼吸道合胞病毒(RSV)mRNA疫苗,通过自主开发冻干工艺,候选产品已在2–8℃保存超过24个月,各项关键质量指标稳定,预计效期可达36个月,显著提升在基层医疗单位的可及性与便利性。上述平台技术也将应用到纳美信后续管线开发中。
临床前研究数据显示,NR222在棉鼠攻毒模型中展现出优于已上市重组蛋白疫苗的中和抗体水平与保护效力,且安全性良好。2025年5月,该项目正式启动I期临床研究,目前已完成I期临床全部受试者入组和接种工作。
公司也在积极推进治疗性管线布局,重点探索HSV-2(Ⅱ型单纯疱疹病毒)等病毒感染的mRNA疫苗解决方案,并持续拓展mRNA技术在自免、肿瘤等领域的应用潜力。未来三年内,计划推动更多治疗性产品项目进入临床阶段,逐步形成差异化、梯队化的研发管线布局。
PART.02
康华生物:
传统疫苗龙头的技术跃迁与协同契机
成立于2004年的康华生物,是国内首家生产并销售人二倍体细胞狂犬病疫苗的企业。该产品自2014年上市以来,凭借免疫原性好、安全性高和免疫持久性强等特点,曾被世界卫生组织(WHO)列为狂犬病疫苗的“金标准”。
2025年11月,上海生物医药并购基金通过上海万可欣生物科技合伙企业(有限合伙)战略并购康华生物,持股比例达21.91%,标志着康华生物正式进入全新发展阶段。
康华生物重组六价诺如病毒疫苗已获中国、美国和澳大利亚临床许可,展现出一定的研发能力。未来,康华生物将在mRNA、重组蛋白/VLP、多糖蛋白结合、新型佐剂等多个前沿疫苗平台展开布局。
然而,要真正实现从“大单品”向“多产品”的跨越,完全依靠自主探索需要较长周期。尤其是在mRNA这类多学科交叉融合的新兴技术领域,快速构建自主能力面临诸多挑战。
因此,拥有成熟mRNA技术平台、已完成临床准入、在研管线储备丰富且具备冻干制剂工艺的纳美信生物,成为理想的整合对象。双方在技术路径、发展阶段与战略目标上的高度互补,为此次合作奠定了坚实基础。
PART.03
共筑mRNA疫苗
“研发-生产-市场”闭环
作为一个刚进入临床研究阶段的Biotech,纳美信生物仍将面临研发注册上市、大规模GMP生产设施的建设、疫苗生产许可证资质的获批,以及全球化运营体系的搭建等诸多挑战。而这些,恰恰是康华生物所擅长的地方。
康华生物现有龙泉、温江两大生产和研发基地,在温江建有14,000平米的研发、中试、质控实验室,具备成熟的病毒疫苗生产工艺与质量管理体系。作为国内首家推出人二倍体细胞狂犬病疫苗的企业,其产品凭借扎实的临床数据,在安全性和有效性上表现突出。依托在人用狂犬病疫苗领域的长期布局,康华生物已形成覆盖全国数千家疾控中心的专业化学术推广体系疾控中心,品牌影响力深厚。
2024年1月,康华生物与HilleVax就重组六价诺如病毒疫苗签署《独家许可协议》,交易金额包括首付款1,500万美元,最高2.555亿美元的开发里程碑和销售里程碑款项,充分展现出公司领先的研发创新实力。
康华生物也将进一步发挥上海作为国内生物药创新桥头堡的战略作用。依托纳美信生物在上海的研发基地及康华生物的产业资源,双方将共同推动与高校、科研院所、临床机构及产业链上下游企业的深度协同。通过联合攻关、人才流动与平台共享,提升区域创新体系的整体效能。
同时,以上海为支点,双方还将积极探索国际化研发路径,推进与海外研究机构、CRO平台及监管机构的技术交流与项目合作,助力mRNA疫苗和治疗性药物在全球范围内的注册申报与市场布局,为中国本土疫苗创新走向国际舞台带来更多可能。
正如纳美信创始人邓明所言:“此次并购为我们的创新技术提供了更广阔的价值实现平台。”这不是终点,而是起点——只有将实验室里的科学突破,转化为万千大众可用、可及的公共健康产品,才算真正完成了创新的闭环。
回望过去几年,mRNA技术因新冠疫情迎来爆发式关注,催生了大量初创企业。但随着新冠红利退去,资本市场逐步回归理性,行业进入价值重塑期。如今,mRNA产业的发展不再依赖单一热点驱动,而是真正回归科学本质:唯有技术创新跨越概念验证门槛,具备明确的临床价值与产业化可行性,才能获得持续发展空间。
本次并购整合恰逢其时。纳美信与康华生物的合作,不仅仅是两家企业之间的资源互补,更是中国mRNA产业演进路径的一次具象呈现:当源头创新能力遇上成熟的产业化体系,从靶点设计到冻干制剂的技术链路,得以通过GMP生产、注册申报和商业化网络被完整打通。
mRNA技术的价值,从来不止于一款高效的新冠疫苗;其真正的潜力,在于能否解决那些长期未被满足的临床需求——从RSV导致的婴幼儿重症肺炎,到肿瘤个体化治疗的响应率瓶颈,再到慢性病毒感染的治疗突破。当基础研究、技术平台与产业能力开始系统性对接,中国mRNA创新的下一程,才刚刚开始。
编辑|施静怡
>>>查看更多:股市要闻