文章来源:医药精英论坛,未经械友授权不得转载
到年底了,这家企业因违规生产被罚千万!年终奖没了。
12月24日深夜,创业板上市公司天益医疗(301097)一则公告,因“生产违规”,公司被拟罚没超1400万元,7170套高风险三类医疗器械全部没收。
这家号称“要做全球第三家全产品线”的上市医企,为啥会犯这种低级错误!
而且,这罚款比它前三季度净利润还多了近400万。

先简单说说天益医疗这家公司:
作为总部位于宁波的高新技术企业,它深耕医疗器械领域多年,是国内较早专注血液净化及病房护理领域医用高分子耗材的企业,还被列为国家级专精特新“小巨人”企业。
公司核心产品就包括这次违规的体外循环血路,拥有超过200种规格型号,也是国内首家获得CRRT专用管路注册证书的企业。

其产品不仅覆盖国内31个省份、超千家医院,还出口至亚洲、欧洲等多个地区,合作客户包括费森尤斯医疗、百特医疗等国际龙头,2022年在深交所创业板上市(证券代码:301097)。
刚扩张就踩雷,高风险器械的红线碰不得
让天益医疗这次栽跟头的,是血液净化装置的体外循环血路,就是肾病患者做透析时的“血液通道”,属于国家重点盯防的三类医疗器械。
三类器械是什么概念?
是和心脏支架、人工瓣膜同级别的“高风险产品”,注册时的技术标准(型号、材质、安全性能)严格遵守“铁规矩”,改一个配件、调一个参数,都算违规。
但天益医疗犯了个 “糊涂”:为了迎合市场需求、适配临床机型,造出了和注册要求不一致的血路产品。

这事怎么发生的?
宁波市市监局的调查结论写道:
天益医疗不是没收到生产标准——销售部、生产车间的文件柜里,都躺着注册技术要求。但架不住“市场需求”:
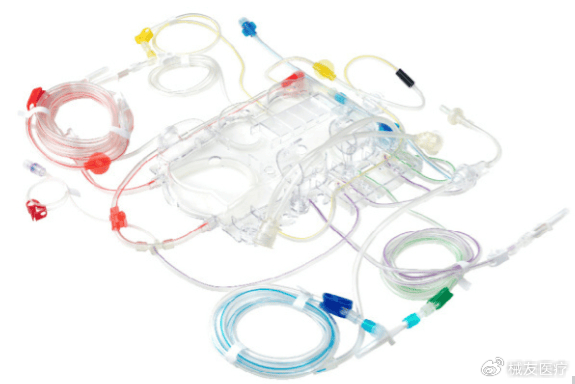
我们可以猜测,医院说“你们的血路和我们的透析机不配套”,销售就催生产“改改参数凑合用”,最后生产部真就照着“非注册标准”,造出了7170套血路产品。
这不是“小失误”,这直接违反了《医疗器械监督管理条例》,构成 “未按经注册的产品技术要求组织生产” 的违法行为。
从监管调查结论和事件来看,这次违规事件中,生产控制部、生产车间、销售部是核心责任部门,对应岗位大概率会被追责,其中生产控制部是主要责任部门,年终奖肯定是没了。

医疗圈因为“三类器械违规生产”栽跟头的,不在少数。
2023年,某上市械企因“人工晶体生产未按注册标准检测”,被没收2000余套产品+罚没1200万;
2024年,江苏一家透析耗材企业,同样因“血路产品改规格”,被罚800万+停产整顿3个月。
罚得重吗?行业里这已经是“从轻发落”
天益医疗这次的罚单,其实是“减轻处罚”后的结果:
监管部门考虑到它是“初次违法”,而且案发后立刻召回产品、配合调查、主动整改,才没直接停产,要是换成屡犯,或者产品出了临床事故,可能连生产许可证都保不住。
看看罚单明细:
直接罚掉了它前三季度2009万的净利润近七成。

刚花大价钱扩张,怎么会栽在这个低级错误
今年9月,天益医疗刚高调宣布:花1199万欧元收购了意大利Bellco的CRRT业务,拿到了欧洲市场的生产线和品牌,号称“要和费森尤斯、万益特抢全球市场”。
刚刚开始要国际化、扩产品线,却在“生产合规”这个最基础的环节掉了链子,医院要什么就改什么,订单比合规重要?

但医疗行业不一样:合规是生存底线,没了底线,再大的盘子也端不住。
医疗器械关乎着生命健康,合规不是“成本”,是对生命的敬畏。天益医疗花钱买教训吧。
注:以上内容仅供参考,不构成投资建议,本文中对官方政策的相关解读,仅代表本平台观点,内容以官方文件为准。
>>>查看更多:股市要闻